La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha anunciado la retirada de un popular medicamento para los ojos al detectar un defecto de calidad en la fabricación de este producto. Se trata de un colirio que se usa para tratar síntomas oculares de la conjuntivitis y de la alergia estacional. El hecho de haber detectado un defecto en la calidad de fabricación podría comprometer su esterilidad y provocar infecciones oculares.
Debido a esto, la AEMPS ha ordenado la retirada del mercado de tres lotes del medicamento Ketobrill 0,25 mg/ml colirio en envase unidosis. El defecto de calidad en la fabricación de este producto consiste en la reutilización de filtros estériles sin que la práctica esté validada.
Este defecto no supone ningún tipo de riesgo vital para el paciente, pero podría comprometer la esterilidad del producto y provocar infecciones oculares. Es por eso precisamente por lo que se recomienda a las personas que hayan adquirido este colirio que lo devuelvan a la farmacia o al punto de venta donde se haya comprado. Para ello se deberá comprobar el número de lote y la fecha de caducidad del envase.
Los lotes retirados del medicamento para los ojos por la AEMPS
Han retirado un total de tres lotes de medicamentos que tenían este defecto. Los tres lotes son los siguientes:
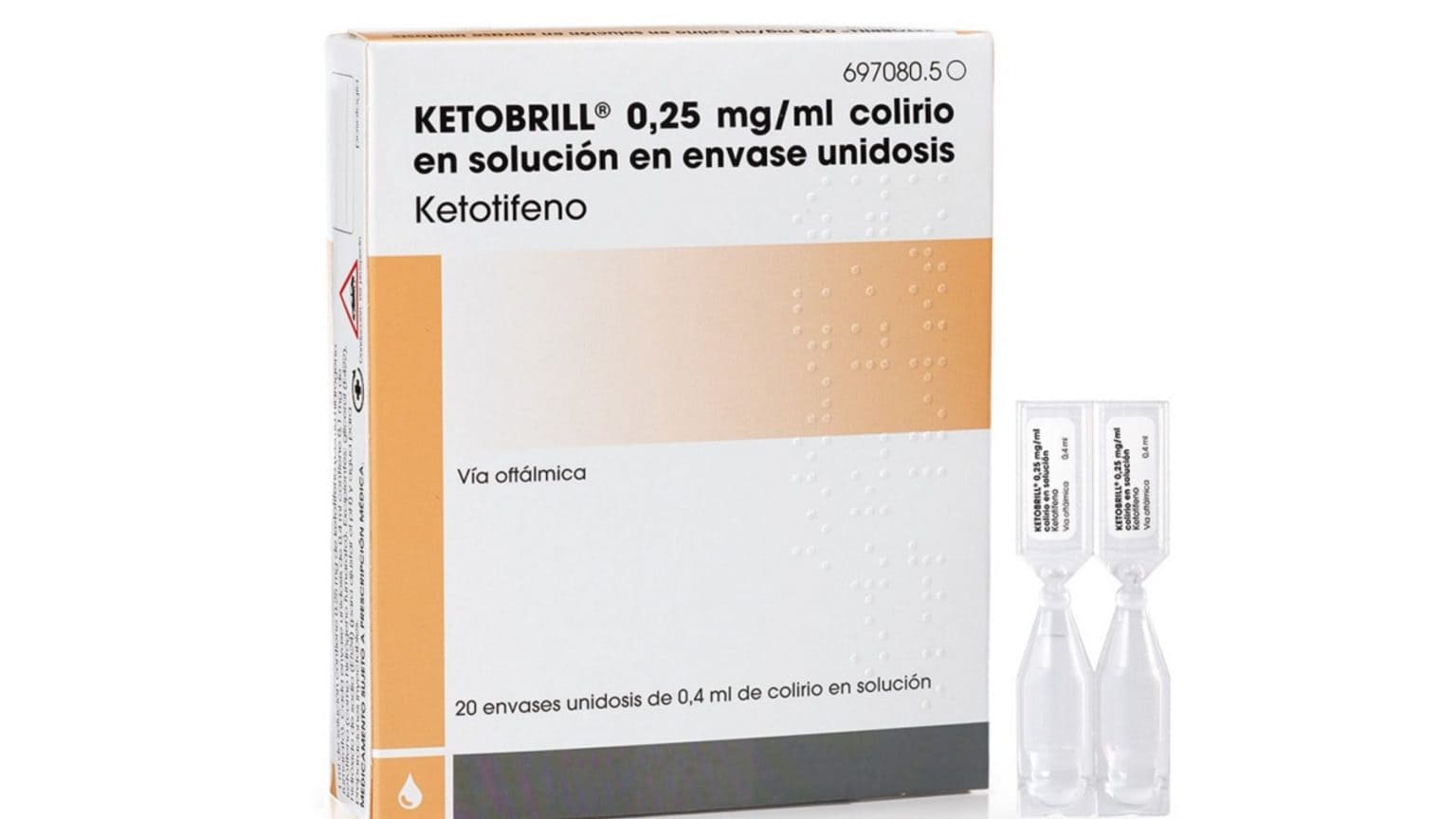
- Lote: 21J004, fecha de caducidad 31/08/2023.
- Lote: 22C049, fecha de caducidad 28/02/2024.
- Lote: 22D022, fecha de caducidad 31/03/2024.
Los lotes han sido fabricados por la empresa Pharma Stulln, que es la titular de la autorización de comercialización del medicamento. La AEMPS ha calificado el defecto como clase 2, lo que quiere decir que podría tener consecuencias para la salud del paciente, aunque no graves. La agencia ha insistido a las comunidades autónomas que realicen un seguimiento de la retirada del producto. Además, ha solicitado al laboratorio que adopte las medidas necesarias para evitar que se repita este suceso.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) recuerda tanto a profesionales de la salud como a ciudadanos la posibilidad de notificar cualquier sospecha de reacción adversa o problema relacionado con el uso de medicamentos a través del Sistema Español de Farmacovigilancia o utilizando el formulario electrónico disponible en su sitio web.
Este incidente marca la segunda ocasión en el año en que se retira un colirio debido a un defecto de calidad. En febrero, la AEMPS emitió una orden de retirada de múltiples lotes del medicamento Oftacilox 3 mg/ml colirio en solución, utilizado para tratar infecciones bacterianas oculares, debido a la presencia de partículas visibles en algunas unidades. En ese caso, el defecto fue categorizado como de clase 1, el más severo, ya que conlleva el riesgo de causar daños irreversibles en la visión.
